Ο καρκίνος, ένας από τους μεγαλύτερους εχθρούς της υγείας του παγκόσμιου πληθυσμού, μοιάζει συχνά με τον γόρδιο δεσμό, ένα μπερδεμένο άλυτο κουβάρι, του οποίου την άκρη προσπαθούν να βρουν άοκνα οι επιστήμονες. Εναν σφιχτό κόμπο στον οποίο «μπλέκονται» πλείστοι καρκινικοί τύποι και υπότυποι, οι οποίοι ζητούν εξειδικευμένες, στοχευμένες λύσεις προκειμένου να αντιμετωπιστούν. Για αυτό και οι προσπάθειες να φωτιστεί η… αρχή του καρκινικού μίτου, οι μηχανισμοί εκείνοι που οδηγούν εξαρχής στην καρκινογένεση, ελπίζεται ότι θα συμβάλουν σημαντικά στη λύση του γόρδιου δεσμού που ταλαιπωρεί εκατομμύρια άτομα παγκοσμίως.
Εναν τέτοιο νέο νευραλγικό μηχανισμό αποκάλυψαν πρόσφατα, με δημοσίευσή τους στο έγκριτο επιστημονικό περιοδικό «Τhe Journal of Cell Biology» (έχει ήδη γίνει η online δημοσίευση ενώ έπεται η έντυπη δημοσίευση στο τεύχος Νοεμβρίου), ερευνητές του Τμήματος Βιολογίας του Πανεπιστημίου Κρήτης με επικεφαλής τον αναπληρωτή καθηγητή δρα Γεώργιο Ζάχο.
Η δημοσίευση αυτή, στην οποία κύρια ερευνήτρια ήταν η δρ Ελένη Πετσαλάκη και συμμετέχουσες ερευνήτριες οι κυρίες Σοφία Μπαλαφούτη και Αθηνά Κυριαζή, συμβάλλει στην κατανόηση σχετικά με το πώς δημιουργούνται πολλές μορφές καρκίνου ανοίγοντας παράλληλα δρόμους για ανάπτυξη νέων στοχευμένων θεραπειών εναντίον τους.
«Tα μόρια του DNA, τα οποία μοιάζουν με μακριές κλωστές, μπλέκονται μεταξύ τους και σχηματίζουν «γέφυρες» DNA. Oi γέφυρες αυτές μπορούν να σπάσουν προκαλώντας βλάβες στο DNA και καρκινογένεση».
Οι «γέφυρες» του DNA
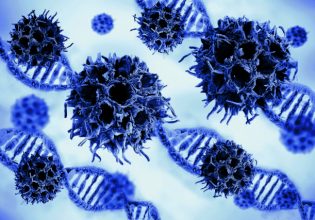
Ο μηχανισμός που έφεραν στο φως οι έλληνες ερευνητές με χρηματοδότηση από τη Fondation Santé και το Ελληνικό Ιδρυμα Ερευνας & Καινοτομίας (ΕΛ.ΙΔ.Ε.Κ.) βοηθά τα ανθρώπινα κύτταρα να αναγνωρίζουν «τοξικές» δομές του DNA, τις λεγόμενες «γέφυρες DNA», οι οποίες μπορούν να οδηγήσουν σε καρκινογένεση. Οπως εξηγεί στο ΒΗΜΑ-Science o δρ Ζάχος, «για να αναπτυχθεί και να συντηρηθεί ο ανθρώπινος οργανισμός, τα κύτταρά του πολλαπλασιάζονται χιλιάδες φορές κατά τη διάρκεια της ζωής μας. Συγκεκριμένα κάθε κύτταρο διπλασιάζει το DNA του και το μοιράζει σε δύο κύτταρα-απογόνους με απόλυτη ακρίβεια, με μια διαδικασία που ονομάζεται κυτταρική διαίρεση. Ωστόσο, σπάνια, τα μόρια του DNA, τα οποία μοιάζουν με μακριές κλωστές, μπλέκονται μεταξύ τους και σχηματίζουν «γέφυρες» DNA που ενώνουν τα κύτταρα-απογόνους. Οταν αυτό συμβεί, οι γέφυρες αυτές μπορούν να σπάσουν προκαλώντας βλάβες στο DNA και καρκινογένεση».
Προκειμένου λοιπόν να προστατευθούν από την καρκινογένεση, τα υγιή κύτταρα του σώματός μας σταματούν την κυτταρική διαίρεση όταν δημιουργούνται τέτοιες γέφυρες (γέφυρες χρωματίνης), ωστόσο το πώς ακριβώς συμβαίνει αυτό δεν είχε έως τώρα καταστεί κατανοητό.
Εικόνα δύο ανθρώπινων καρκινικών κυττάρων που ενώνονται με γέφυρα DNA (μεγάλο βέλος), η οποία ελήφθη με συνεστιακή μικροσκοπία υψηλής ανάλυσης. Τα ένθετα δείχνουν τον κόμπο του DNA (μικρό βέλος) καθώς και πρωτεΐνες που εντοπίζονται επάνω σε αυτόν για να εμποδίσουν το σπάσιμο της γέφυρας (δρ. Πετσαλάκη και καθηγητής Γεώργιος Ζάχος, Πανεπιστήμιο Κρήτης)
Η πρωτεΐνη και οι κόμποι
Οι ερευνητές του Πανεπιστημίου Κρήτης ανακάλυψαν ότι τα μπλεγμένα μόρια DNA σχηματίζουν «κόμπους», τους οποίους ανιχνεύει μια πρωτεΐνη η οποία ονομάζεται Τοποϊσομεράση 2. Η δρ Πετσαλάκη περιγράφει ότι «η πρωτεΐνη αυτή συνδέεται στους κόμπους του DNA των γεφυρών και προσπαθεί να τους λύσει. Εάν δεν τα καταφέρει, «μαρκάρει» τον κόμπο του DNA κάνοντας δύο μικρά κοψίματα επάνω στο μπλεγμένο DNA. Τα κοψίματα αυτά λειτουργούν ως σημάδι για να προσελκύσουν άλλες πρωτεΐνες οι οποίες σταματούν την κυτταρική διαίρεση και εμποδίζουν το σπάσιμο των γεφυρών DNA – προσελκύουν αρχικώς τη σηματοδοτική πρωτεΐνη Rad17 και ακολούθως τις σηματοδοτικές πρωτεΐνες του κυττάρου MRN, ATM, Chk2 και INCENP».
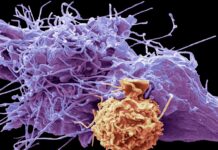
Το συγκεκριμένο σηματοδοτικό μονοπάτι όμως δεν είναι απαραίτητο μόνο για την επιβίωση των υγιών κυττάρων αλλά και των καρκινικών. Και αυτό επιβεβαίωσαν μέσα από πειράματα σε καλλιέργειες καρκινικών κυττάρων του παχέος εντέρου και του επιθηλίου του τραχήλου της μήτρας και του νεφρού οι έλληνες επιστήμονες. «Είδαμε ότι τα καρκινικά κύτταρα σχηματίζουν και εκείνα γέφυρες και κόμπους προκειμένου να προστατευθούν και πιστεύουμε ότι η αναστολή της δράσης πρωτεϊνών αυτού του μονοπατιού μέσω της χορήγησης φαρμάκων θα μπορούσε να οδηγήσει σε θάνατο πολλούς τύπους καρκινικών κυττάρων» σημειώνει ο δρ Ζάχος.

O επικεφαλής της ερευνητικής ομάδας του Πανεπιστημίου Κρήτης που διεξήγαγε τη νέα μελέτη δρ Γεώργιος Ζάχος.
Οι εξαιρέσεις
Υπάρχουν και μορφές καρκίνου που δεν… ασχολούνται με κόμπους; Υπάρχουν τύποι στους οποίους δεν υφίσταται ο μηχανισμός που έφερε στο φως η ελληνική ερευνητική ομάδα; «Ο μηχανισμός αυτός δεν φαίνεται να λειτουργεί σε μορφές καρκίνου που προέρχονται από είδη γεφυρών DNA οι οποίες δεν δημιουργούν κόμπους. Πρόκειται για γέφυρες που δημιουργούνται σε κύτταρα τα οποία έχουν γεράσει και σχηματίζονται με διαφορετικό μηχανισμό – στις γέφυρες αυτές τα τελομερή, τα άκρα δηλαδή των χρωμοσωμάτων, κολλούν μεταξύ τους. Στη συγκεκριμένη περίπτωση δεν λειτουργεί ο προστατευτικός μηχανισμός που εμποδίζει το σπάσιμο των γεφυρών» απαντά ο καθηγητής. Ουσιαστικώς ο μηχανισμός των γεφυρών DNA και των κόμπων δεν λειτουργεί σε πιο ηλικιωμένα άτομα που διαθέτουν πιο γηρασμένα κύτταρα. «Δεν γνωρίζουμε αν υπάρχει στα άτομα αυτά κάποιος άλλος προστατευτικός μηχανισμός ενάντια στην καρκινογένεση. Πάντως δεν είναι τυχαίο ότι τα πιο ηλικιωμένα άτομα είναι πιο επιρρεπή σε καρκίνους» συμπληρώνει ο δρ Ζάχος.
Οι νέες προοπτικές
Επόμενο βήμα για την ερευνητική ομάδα, διά στόματος του επικεφαλής της, είναι να διεξαχθούν αντίστοιχες μελέτες σε σφαιρίδια καρκινικών κυττάρων. «Τα σφαιρίδια καρκινικών κυττάρων αποτελούν τρισδιάστατες καλλιέργειες καρκινικών κυττάρων που μιμούνται τους όγκους – έχουν τις ιδιότητες των όγκων και προσφέρονται για πιο ακριβή συμπεράσματα καθώς έχουμε πολύ καλύτερη προσομοίωση του τι συμβαίνει στον ανθρώπινο οργανισμό όταν δημιουργούνται καρκινικοί όγκοι. Πρώτος στόχος μας είναι η μελέτη του καρκίνου του παχέος εντέρου και του νεφρού».
Συνολικά, σύμφωνα με τους ερευνητές, η μελέτη τους ανοίγει καινούργιους δρόμους στην κατανόηση μιας από τις κύριες αιτίες της μοριακής προέλευσης του καρκίνου – γεγονός που με τη σειρά του χαράσσει νέα αντικαρκινικά μονοπάτια. «Τα αποτελέσματά μας είναι τα πρώτα που περιγράφουν πώς τα κύτταρα του σώματός μας αισθάνονται την ύπαρξη των γεφυρών DNA ώστε να τις αντιμετωπίσουν και χαρτογραφούν έναν βασικό μηχανισμό που προστατεύει από καρκινογένεση» αναφέρει ο καθηγητής Ζάχος και η μεταδιδακτορική ερευνήτρια δρ Πετσαλάκη συμπληρώνει από την πλευρά της ότι «ο μηχανισμός που ανακαλύψαμε, μπορεί να αποτελέσει την αχίλλειο πτέρνα για πολλές μορφές καρκίνου στο μέλλον». Μάκαρι αυτό το πιθανό «τρωτό σημείο» του καρκίνου που ανακάλυψαν οι έλληνες ερευνητές να «ρίξει γέφυρες» προς νέες θεραπείες, οι οποίες θα βοηθήσουν εκατομμύρια ασθενείς στα χρόνια που έρχονται.
Απώτερος σκοπός η ανάπτυξη στοχευμένων φαρμάκων
Θα αναρωτιόταν κάποιος και ευλόγως πώς η νέα ελληνική μελέτη θα μπορούσε κάποια ημέρα να μεταφραστεί σε χειροπιαστές θεραπείες προς όφελος των ασθενών με καρκίνο. Το καίριο αυτό ερώτημα θέτουμε και στον κ. Ζάχο. Οπως απαντά, «τα ευρήματά μας μαρτυρούν ότι θα μπορούσαμε στο μέλλον να στοχεύουμε πρωτεΐνες που ελέγχουν τον μηχανισμό τον οποίο ανακαλύψαμε. Εάν στοχεύσουμε επιλεκτικά αυτό το μονοπάτι στα καρκινικά κύτταρα θα καταφέρουμε να τους προκαλέσουμε μεγάλες βλάβες και να τα οδηγήσουμε στον θάνατο. Ουσιαστικός σκοπός μας είναι δηλαδή να καταστήσουμε ευάλωτα τα καρκινικά κύτταρα με φαρμακευτική στόχευση καταλύοντας τον μηχανισμό των γεφυρών που τα προστατεύει».
Ενα πρώτο μεγάλο ερώτημα είναι το πώς θα προστατεύονται τα υγιή κύτταρα, στα οποία επίσης υπάρχει ο ίδιος μηχανισμός, σε περίπτωση χορήγησης φαρμάκων που θα τον στοχεύουν. Σύμφωνα με τον καθηγητή, «κατ’ αρχάς τα φυσιολογικά κύτταρα δεν διαιρούνται με τους ίδιους ταχείς ρυθμούς όπως τα καρκινικά, οπότε εξαρχής δεν θα είναι τόσο ευάλωτα στα φάρμακα που θα βασίζονται σε αυτή τη φιλοσοφία. Παράλληλα όμως, απώτερος στόχος είναι η ανάπτυξη στοχευμένων φαρμάκων τα οποία θα επικεντρώνονται στα καρκινικά κύτταρα προκαλώντας τους σημαντικές βλάβες ώστε να εξοντώνονται και δεν θα επηρεάζουν τόσο τα υγιή κύτταρα».
Ενα δεύτερο μεγάλο ερώτημα αφορά το αν υπάρχουν ήδη κάποια φάρμακα που στοχεύουν πρωτεΐνες του συγκεκριμένου μονοπατιού, τα οποία και θα μπορούσαν να δοκιμαστούν ή αν απαιτείται η ανάπτυξη νέων φαρμάκων από το μηδέν. «Για την Τοποϊσομεράση 2 υπάρχουν εδώ και χρόνια φάρμακα – ονομάζονται δηλητήρια της Τοποϊσομεράσης 2 –, τα οποία χορηγούνται για πολλές μορφές καρκίνου όπως του μαστού, των ωοθηκών, του στομάχου. Τα φάρμακα αυτά απενεργοποιούν μεν την Τοποϊσομεράση 2, έχει όμως αποδειχθεί ότι προκαλούν βλάβες στο DNA. Ετσι ενώ χρησιμοποιούνται στην κλινική πράξη, η χρήση τους γίνεται με φειδώ καθώς έχουν ως κύριες παρενέργειες την εμφάνιση λευχαιμιών, νευρολογικών και καρδιολογικών προβλημάτων. Στη μελέτη μας δείξαμε ότι τα δηλητήρια της Τοποϊσομεράσης 2 δεν είναι αποτελεσματικά ενάντια στον μηχανισμό που ανακαλύψαμε. Ωστόσο προτείνουμε χρήση άλλων φαρμάκων τα οποία δεν έχουν δοκιμαστεί συστηματικά σε ανθρώπους και ονομάζονται αναστολείς της Τοποϊσομεράσης 2. Δρουν με διαφορετικό τρόπο και απενεργοποιούν τον μηχανισμό που περιγράφουμε χωρίς να προκαλούν βλάβες στο DNA. Εκτιμούμε ότι πρέπει να στρέψουμε το ενδιαφέρον μας προς τους αναστολείς της Τοποϊσομεράσης 2 για να αποκτήσουμε αποτελεσματικότερα και ασφαλέστερα ενάντια σε πολλές μορφές καρκίνου φάρμακα στο μέλλον».
Μάλιστα οι ερευνητές διεξήγαγαν πειράματα σε καλλιέργειες καρκινικών κυττάρων του παχέος εντέρου καθώς και του επιθηλίου του τραχήλου της μήτρας και του νεφρού χρησιμοποιώντας τόσο δηλητήρια της Τοποϊσομεράσης 2 όσο και αναστολείς της πρωτεΐνης και αυτή τη στιγμή βρίσκονται σε φάση αξιολόγησης των αποτελεσμάτων.
Μια άλλη προσέγγιση που θα μπορούσε να ακολουθηθεί, χωρίς χορήγηση φαρμάκων, θα ήταν η παρέμβαση στα microRNA των πρωτεϊνών οι οποίες εμπλέκονται στον μηχανισμό που μόλις ανακαλύφθηκε, καταλήγει ο κ. Ζάχος.

Από αριστερά, ο επικεφαλής της ερευνητικής ομάδας αναπληρωτής καθηγητής του Τμήματος Βιολογίας στο Πανεπιστήμιο Κρήτης Γεώργιος Ζάχος, η κύρια ερευνήτρια της νέας μελέτης δρ Ελένη Πετσαλάκη και η συμμετέχουσα ερευνήτρια κυρία Σοφία Μπαλαφούτη.
Απώτερος στόχος η ανάπτυξη στοχευμένων φαρμάκων
Θα αναρωτιόταν κάποιος και ευλόγως πώς η νέα ελληνική μελέτη θα μπορούσε κάποια ημέρα να μεταφραστεί σε χειροπιαστές θεραπείες προς όφελος των ασθενών με καρκίνο. Το καίριο αυτό ερώτημα θέτουμε και στον κ. Ζάχο. Οπως απαντά, «τα ευρήματά μας μαρτυρούν ότι θα μπορούσαμε στο μέλλον να στοχεύουμε πρωτεΐνες που ελέγχουν τον μηχανισμό τον οποίο ανακαλύψαμε. Εάν στοχεύσουμε επιλεκτικά αυτό το μονοπάτι στα καρκινικά κύτταρα θα καταφέρουμε να τους προκαλέσουμε μεγάλες βλάβες και να τα οδηγήσουμε στον θάνατο. Ουσιαστικός σκοπός μας είναι δηλαδή να καταστήσουμε ευάλωτα τα καρκινικά κύτταρα με φαρμακευτική στόχευση καταλύοντας τον μηχανισμό των γεφυρών που τα προστατεύει».
Ενα πρώτο μεγάλο ερώτημα είναι το πώς θα προστατεύονται τα υγιή κύτταρα, στα οποία επίσης υπάρχει ο ίδιος μηχανισμός, σε περίπτωση χορήγησης φαρμάκων που θα τον στοχεύουν. Σύμφωνα με τον καθηγητή, «κατ’ αρχάς τα φυσιολογικά κύτταρα δεν διαιρούνται με τους ίδιους ταχείς ρυθμούς όπως τα καρκινικά, οπότε εξαρχής δεν θα είναι τόσο ευάλωτα στα φάρμακα που θα βασίζονται σε αυτή τη φιλοσοφία. Παράλληλα όμως, απώτερος στόχος είναι η ανάπτυξη στοχευμένων φαρμάκων τα οποία θα επικεντρώνονται στα καρκινικά κύτταρα προκαλώντας τους σημαντικές βλάβες ώστε να εξοντώνονται και δεν θα επηρεάζουν τόσο τα υγιή κύτταρα».
Ενα δεύτερο μεγάλο ερώτημα αφορά το αν υπάρχουν ήδη κάποια φάρμακα που στοχεύουν πρωτεΐνες του συγκεκριμένου μονοπατιού, τα οποία και θα μπορούσαν να δοκιμαστούν ή αν απαιτείται η ανάπτυξη νέων φαρμάκων από το μηδέν. «Για την Τοποϊσομεράση 2 υπάρχουν εδώ και χρόνια φάρμακα – ονομάζονται δηλητήρια της Τοποϊσομεράσης 2 -, τα οποία χορηγούνται για πολλές μορφές καρκίνου όπως του μαστού, των ωοθηκών, του στομάχου. Τα φάρμακα αυτά απενεργοποιούν μεν την Τοποϊσομεράση 2, έχει όμως αποδειχθεί ότι προκαλούν βλάβες στο DNA. Ετσι ενώ χρησιμοποιούνται στην κλινική πράξη, η χρήση τους γίνεται με φειδώ καθώς έχουν ως κύριες παρενέργειες την εμφάνιση λευχαιμιών, νευρολογικών και καρδιολογικών προβλημάτων. Στη μελέτη μας δείξαμε ότι τα δηλητήρια της Τοποϊσομεράσης 2 δεν είναι αποτελεσματικά ενάντια στον μηχανισμό που ανακαλύψαμε. Ωστόσο προτείνουμε χρήση άλλων φαρμάκων τα οποία δεν έχουν δοκιμαστεί συστηματικά σε ανθρώπους και ονομάζονται αναστολείς της Τοποϊσομεράσης 2. Δρουν με διαφορετικό τρόπο και απενεργοποιούν τον μηχανισμό που περιγράφουμε χωρίς να προκαλούν βλάβες στο DNA. Εκτιμούμε ότι πρέπει να στρέψουμε το ενδιαφέρον μας προς τους αναστολείς της Τοποϊσομεράσης 2 για να αποκτήσουμε αποτελεσματικότερα και ασφαλέστερα ενάντια σε πολλές μορφές καρκίνου φάρμακα στο μέλλον».
Μάλιστα οι ερευνητές διεξήγαγαν πειράματα σε καλλιέργειες καρκινικών κυττάρων του παχέος εντέρου καθώς και του επιθηλίου του τραχήλου της μήτρας και του νεφρού χρησιμοποιώντας τόσο δηλητήρια της Τοποϊσομεράσης 2 όσο και αναστολείς της πρωτεΐνης και αυτή τη στιγμή βρίσκονται σε φάση αξιολόγησης των αποτελεσμάτων.
Μια άλλη προσέγγιση που θα μπορούσε να ακολουθηθεί, χωρίς χορήγηση φαρμάκων, θα ήταν η παρέμβαση στα microRNA των πρωτεϊνών οι οποίες εμπλέκονται στον μηχανισμό που μόλις ανακαλύφθηκε, καταλήγει ο κ. Ζάχος.
Έντυπη έκδοση Το Βήμα
[Πηγή:]www.in.gr